医薬品製造・販売業 D社 様
- 要約
-
30年間保存しなければならない臨床試験データを長期保存できるソリューションを探していた
-
データの作成時点から消失・漏えい・改ざんを防ぎつつ、長期にわたり継続可能な運用を提供できるNXワンビシアーカイブズへ委託
-
データの機密性・安全性を確保しつつ、コストや手間の削減が可能に
導入背景
D社は、江戸時代創業の企業を源流としている製薬企業。
製薬企業にとって、臨床試験データは、医薬品の研究開発の要ともいえる、重要なデータである。
臨床試験データは長期の保存が求められるが、企業によりその保存年限は様々で、10年、30年のところもあれば永年保存している企業もある。
また、臨床試験データは従来、紙資料で保存するのが通例であった。しかし、電子カルテに見られるような電子化の流れ、共同治験の普及による試験の多様化・複雑化によってデータの種類や量は増大しており、デジタルデータのまま保存したいという意向が強まっている。
同社では、臨床試験データを30年間保存するよう定めている。また、デジタル形式で作成していることから、データの作成時点から消失・漏えい・改ざんを防ぎつつ、長期保存できるソリューションが求められていた。

成果
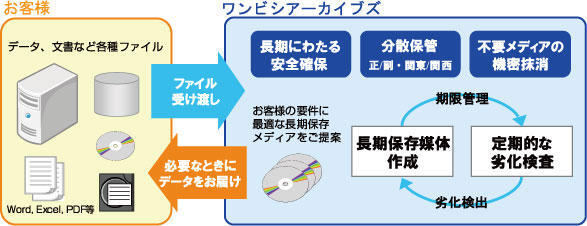
同社では、臨床試験で得られた電子データのアーカイブ(長期保存)をNXワンビシアーカイブズへ委託。以下のような運用で、データの機密性・安全性を確保している。
- D社は、対象データを記録したメディアをNXワンビシアーカイブズ専用車両で搬送
- NXワンビシアーカイブズにて、対象データを長期保存用の記録メディアに移行同じ内容のメディアを計3個(正/副/副)作成し、NXワンビシアーカイブズの情報管理センター2拠点(関東/関西)に保管。それによりデータバックアップの確実性の向上と、災害対策を実現している。
- 定期的に記録メディアの劣化状況を検査し、万一劣化の兆候が見られた場合は別のメディアにデータを移行
データ管理のコンプライアンス強化
電子データへの移行・利用に関する証跡がすべて残されるため、確実性が増し、規制当局からの厳しい監査への対応が容易に。
安全・確実なデータ長期保存体制の確立
担当者や組織に依存することなく、電子データを長期保存できる体制を確立。
コストや手間の削減
長期保存専用のシステム機能やストレージを自社で用意する必要がなく、データ管理部門やIT部門の負担が軽減。
サービスの選定ポイント
- 規格に沿った手法や様々な証跡を記録することによる徹底したアカウンタビリティの確保
- 長期にわたり継続可能な運用をワンストップで提供できる総合力
- 製薬業・金融業・官公庁をはじめ多くのお客様から信頼を受け、GxP
(※)省令対応の実績もあるセキュリティやサービス品質の管理体制
※ GxP Good x Practice の略で、安全性や信頼性を確保することを目的に政府等で制定された基準の総称。 厳しい保管・保存基準が求められる医薬開発関係資料を、適切な環境・体制でお預かりするサービスもご提供しております。
サービスのご案内はこちら
企業概要
医薬品製造・販売
本社所在地:大阪府
従業員数:5,000名以下

